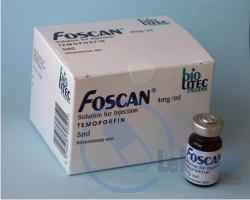
WskazaniaPreparat jest wskazany do paliatywnego leczenia zaawansowanego raka płaskonabłonkowego głowy i szyi u pacjentów, u których zawiodły wcześniej stosowane metody leczenia i u których nie można zastosować radioterapii, leczenia chirurgicznego lub ogólnoustrojowej chemioterapii.DawkowanieTerapia fotodynamiczna z zastosowaniem produktu leczniczego może być prowadzona wyłącznie w specjalistycznych ośrodkach onkologicznych, zapewniających pacjentowi opiekę wszechstronnie wyszkolonego zespołu medycznego oraz nadzór lekarzy mających doświadczenie w prowadzeniu terapii fotodynamicznej. Dawka wynosi 0,15 mg/kg mc. Dzieci i młodzież. Stosowanie produktu leczniczego u dzieci i młodzieży nie jest wskazane.
PrzeciwwskazaniaNadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą. Porfiria lub inne choroby nasilające się pod wpływem światła. Nadwrażliwość na porfiryny. Guzy naciekające duże naczynia krwionośne lub guzy tak położone, że naświetlany obszar bezpośrednio sąsiaduje z dużymi naczyniami krwionośnymi. Zabieg chirurgiczny planowany do przeprowadzenia w okresie najbliższych 30 dni. Współistniejące choroby oczu, które mogą wymagać przeprowadzenia w okresie najbliższych 30 dni badania przy użyciu lampy szczelinowej. Aktualnie prowadzona terapia lekiem zwiększającym wrażliwość na światło.Ostrzeżenia specjalne / Środki ostrożnościSzczególną ostrożność należy zachować w celu uniknięcia wydostania się leku poza naczynie krwionośne w miejscu wstrzyknięcia. Jeżeli dojdzie do wynaczynienia roztworu, miejsce objęte wynaczynieniem powinno być chronione przed dostępem światła przez co najmniej 3 m-ce. Nie stwierdzono by nastrzykiwanie innymi substancjami miejsca objętego wynaczynieniem przynosiło jakiekolwiek korzyści. Niektóre pulsoksymetry mogą emitować światło o długości fali zbliżonej do wymaganej dla fotoaktywacji preparatu. Położenie pulsoksymetrów powinno być zmieniane przynajmniej co 10-15 min., w celu uniknięcia niebezpieczeństwa wystąpienia miejscowych oparzeń skóry. Przez 6 m-cy od zakończenia leczenia preparatem należy unikać długotrwałej ekspozycji ramienia, w które wykonano wstrzyknięcie, na światło słoneczne. Jeżeli planuje się długotrwałe przebywanie na świeżym powietrzu, należy chronić ramię, w które wykonano wstrzyknięcie, okrywając je długim, barwnym rękawem. W okresie 30 dni od podania preparatu nieplanowane lub wynikające z naglących wskazań zabiegi chirurgiczne powinny być wykonywane tylko w razie bezwzględnej konieczności i stwierdzenia, że potencjalna korzyść przeważa ryzyko dla pacjenta. Muszą być zachowywane wszystkie możliwe środki ostrożności zapewniające ochronę pacjenta przed bezpośrednim oświetlaniem lampami chirurgicznymi podczas zabiegu. U wszystkich pacjentów otrzymujących preparat występuje przemijająca nadwrażliwość na światło. W ciągu pierwszych 15 dni po wstrzyknięciu preparatu pacjent musi unikać ekspozycji skóry i oczu na bezpośrednie światło słoneczne lub jaskrawe oświetlenie wewnątrz pomieszczeń. Reakcje nadwrażliwości skóry na światło, występujące podczas terapii preparatem, wywoływane są przez światło widzialne, tak więc środki chroniące przed ultrafioletowym promieniowaniem słonecznym nie stanowią żadnej ochrony przed tymi reakcjami. Ważne jest by pacjenci stopniowo powracali do normalnej ekspozycji na światło. Lekarze muszą pouczyć pacjentów o potrzebie prowadzenia obserwacji i przestrzegania środków ostrożności opisanych w ulotce dla pacjenta. Produkt zawiera etanol (alkohol) w stężeniu 48%, jedna dawka produktu zawiera 4,2 g alkoholu, co odpowiada 84 ml piwa lub 35 ml wina. Jest to dawka szkodliwa dla pacjentów z chorobą alkoholową. Należy to uwzględnić podczas leczenia kobiet w ciąży lub karmiących piersią, dzieci i grup pacjentów wysokiego ryzyka, np. z chorobą wątroby lub padaczką. Ilość alkoholu w produkcie może wpłynąć na działanie innych leków. Ilość alkoholu w produkcie może ograniczać zdolność pacjenta do prowadzenia pojazdów i obsługi maszyn.InterakcjeIstnieje możliwość zaostrzenia wrażliwości skóry na światło, jeżeli temoporfin jest stosowany jednocześnie z innymi substancjami czynnymi uwrażliwiającymi skórę na działanie światła. Zjawisko takie opisywano w przypadku miejscowego stosowania 5-fluorouracylu. Nie obserwowano żadnych innych interakcji. Badania in vitro, prowadzone na ludzkich tkankach wątrobowych, nie wykazały możliwości występowania interakcji z innymi lekami z powodu hamowania przez temoporfin aktywności enzymów cytochromu P-450.Ciąża i laktacjaNie ma danych na temat stosowania temoporfinu u ciężarnych kobiet. Temoporfinu nie wolno stosować w okresie ciąży, jeśli nie jest to bezwzględnie konieczne. Badania prowadzone na zwierzętach wskazują na toksyczne działanie leku we wczesnej ciąży. Potencjalne zagrożenie dla człowieka nie jest nieznane. Dlatego też, kobieta musi unikać zajścia w ciążę w ciągu 3 m-cy po zakończeniu leczenia temoporfinem. Nie wiadomo, czy temoporfin przenika do mleka ludzkiego. Kobietom otrzymującym preparat nie wolno karmić piersią co najmniej przez miesiąc po wstrzyknięciu leku.Działania niepożądaneZakażenia i zarażenia pasożytnicze: (często) miejscowe zakażenie. Zaburzenia krwi i układu chłonnego: (często) niedokrwistość. Zaburzenia żołądka i jelit: (bardzo często) zaparcia; (często) wymioty, owrzodzenia błony śluzowej jamy ustnej, trudności w przełykaniu. Zaburzenia skóry i tkanki podskórnej: (często) pęcherze, rumień, oparzenia, nadmierna pigmentacja skóry, reakcje nadwrażliwości na światło, oparzenia słoneczne, martwica skóry. Zaburzenia ogólne i stany w miejscu podania: (bardzo często) ból w miejscu wstrzyknięcia; ból ten jest przemijający i można go zmniejszyć poprzez spowolnienie szybkości wstrzykiwania leku; (często) gorączka, nudności, reakcje w miejscu wstrzyknięcia, uczucie pieczenia, zawroty głowy. Procedury medyczne i chirurgiczne: (bardzo często) ból, krwawienie, ból w obrębie twarzy, blizny, martwica jamy ustnej, dysfagia, obrzęk twarzy. Ból występujący po leczeniu może wymagać krótkotrwałego zastosowania NLPZ lub opioidowych leków przeciwbólowych; (często) obrzęki, szczękościsk.PrzedawkowanieW razie przedawkowania temoporfinu, leczenie światłem laserowym może wywołać głębszą martwicę guza niż można byłoby to przewidywać po zastosowaniu dawki zalecanej. Naświetlenie guza można przeprowadzić tylko wtedy, gdy potencjalna korzyść uzasadnia możliwe ryzyko rozległej martwicy. Jeżeli guz nie jest naświetlany, musi być zachowana co najmniej 4-tyg. przerwa pomiędzy przedawkowaniem i ponownym podaniem preparatu. Można spodziewać się, że działania niepożądane związane z przedawkowaniem będą ograniczone do reakcji wynikających ze zwiększonej wrażliwości na światło. Ekspozycja na otaczające światło po przedawkowaniu temoporfinu niesie ze sobą zwiększone ryzyko występowania reakcji wynikających ze zwiększonej wrażliwości na światło. Publikowane wyniki badań klinicznych wskazują, że czas trwania i nasilenie wzmożonej wrażliwości na światło po podaniu zalecanej dawki 0,15 mg/kg mc. były o jedną trzecią mniejsze niż po podaniu dawki 0,3 mg/kg mc. Badania prowadzone na zwierzętach ujawniły pewne zmiany hematologiczne i biochemiczne we krwi (zmniejszenie liczby płytek i krwinek czerwonych, zmniejszenie stężenia hemoglobiny, zwiększenie liczby granulocytów obojętnochłonnych, stężenia fibrynogenu, bilirubiny, triglicerydów i cholesterolu). W przypadku przedawkowania temoporfinu wymagana jest ścisła obserwacja pacjenta i pozostawanie w warunkach zmniejszonego oświetlenia. Zanim pacjent powróci do normalnych warunków oświetlenia, musi mieć wykonane skórne testy wrażliwości na światło. Nie są znane żadne specyficzne, ogólne objawy przedawkowania. Należy zastosować leczenie podtrzymujące. Informacje na temat następstw nadmiernej ekspozycji na światło laserowe podczas leczenia są ograniczone. Obserwowano zwiększone uszkodzenia tkanek.DziałanieTen produkt leczniczy został dopuszczony do obrotu zgodnie z procedurą „dopuszczenia w wyjątkowych okolicznościach”. Oznacza to, że ze względu na rzadkie występowanie choroby oraz z powodu ograniczeń naukowych nie było możliwe uzyskanie pełnej informacji dotyczącej korzyści i ryzyka związanych ze stosowaniem tego produktu leczniczego. EMEA dokona przeglądu wszystkich dostępnych nowych informacji o produkcie raz do roku i uzupełni ChPL, jeśli to będzie konieczne. Temporofina jest substancją fotouczulającą stosowaną w terapii fotodynamicznej nowotworów. Aktywność farmakologiczna dożylnie podanego temoporfinu jest inicjowana poprzez fotoaktywację zimnym światłem o długości fali 652 nm. Działanie lecznicze temoporfinu jest następstwem powstawania wysoce reaktywnych form tlenu w procesie zależnym od wewnątrzkomórkowego oddziaływania temoporfinu ze światłem i tlenem.Skład1 ml roztworu zawiera 4 mg temoporfinu.









 Światło
Światło Ciąża - trymestr 1 - Kategoria C
Ciąża - trymestr 1 - Kategoria C Ciąża - trymestr 2 - Kategoria C
Ciąża - trymestr 2 - Kategoria C Ciąża - trymestr 3 - Kategoria C
Ciąża - trymestr 3 - Kategoria C



Komentarze
[ z 0]